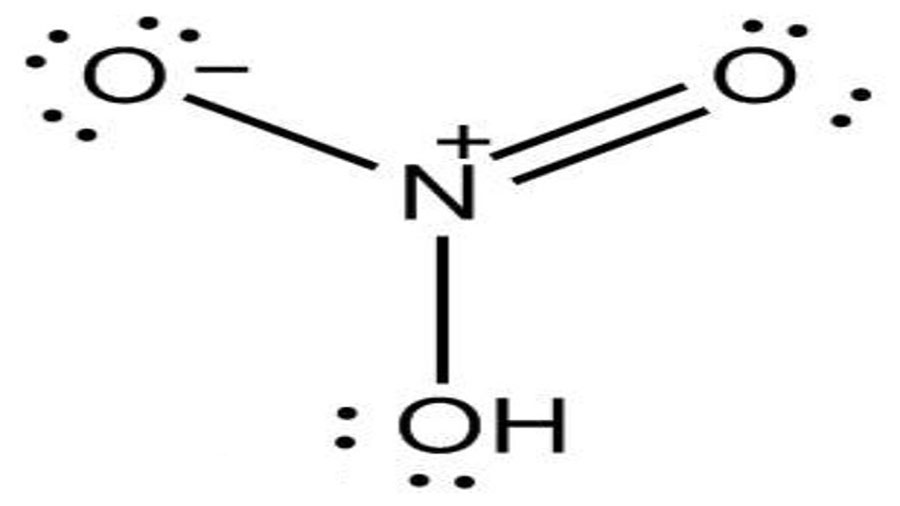
Axit nitric là một axit vô cơ có công thức hóa học HNO3. Axit nitric tinh khiết là chất lỏng, không màu, bốc khói mạnh trong không khí ẩm, nó là một axit mạnh nên HNO3 có rất nhiều ứng dụng trong đời sống. Chúng ta hãy cùng nhau tìm hiểu về hóa chất này nhé.
Thông tin về sản phẩm Axit nitric HNO3
– Nồng độ: 68%
– Xuất xứ: Thái Lan, Hàn Quốc

(HNO3 68% có xuất xứ Hàn Quốc)
– Trạng thái: dạng lỏng
– Quy cách: 35kg/can; 280kg/thùng
Tính chất vật lý và hóa học Của HNO3
Tính chất vật lý của HNO3
– Axit nitric tinh khiết là một chất lỏng không màu và trong suốt, nhưng axit nitric đậm đặc lại có màu vàng nhạt.
– Nó có mùi khó chịu ngột ngạt.
– Khối lượng mol: 63,01214 g/mol (khan) ;81,02742 g/mol ( ngậm1 nước) và 117,05798 g/mol ( ngậm 3 nước).
– Nhiệt độ sôi: 83°C (181°F; 356 K).
– Nhiệt độ nóng chảy: −42°C (−44°F; 231 K).
– Tan trong nước theo bất kì tỉ lệ nào.
– Axit nitric được sử dụng và thường gặp nhất là ở nồng độ 68%.
Tính chất hóa học của HNO3
Thể hiện là một Axit mạnh
– Làm cho quỳ tím hóa thành đỏ
– Tác dụng với oxit kim loại tạo thành muối và nước
- 2HNO3 + CuO → Cu(NO3)2 + H2O
– Tác dụng với bazơ tạo cũng ra sản phẩm là muối và nước
- HNO3 + NaOH → NaNO3 + H2O
- HNO3 + KOH → KNO3 + H2O
– Tác dụng với muối sản phẩm thu được là muối mới và axit mới
- HNO3 + CaCO3 → Ca(NO3)2 + CO2 + H2O
(Công thức phân tử HNO3)
Thể hiện tính oxy hóa
Axit nitric có số oxy hóa cao nhất là +5. Tùy theo tỷ lệ nồng độ, nhiệt độ và chất tham gia phản ứng sản sản phẩm tạo ra cuối cùng có thể gồm nhiều loại và nhiều sản phẩm khử đa dạng như N2, NO, NO2, N2O, NH4NO3
– Tác dụng với hầu hết kim loại trừ ác các kim loại quý (Au, Pt) và một số hợp kim
- Cu + 4HNO3 (đặc) → Cu(NO3)2 + 2NO2↑ + 2H2O
- 3Cu + 8HNO3 (loãng) → 3Cu(NO3)2 + 2NO↑ + 4H2O
- Mg(rắn) + 2HNO3 (dd) → Mg(NO3)2 (dd) + H2 (khí)
– Tác dụng với phi kim
- C + 4HNO3 → CO2↑ + 4NO↑ + 2H2O
- S + 4HNO3 → CO2↑ + 4NO↑ + 2H2O
- P + 5HNO3 → H3PO4 + 5NO2↑ + H2O
– Tác dụng với nhiều hợp chất khác nhau
- 3H2S + 2HNO3 (>5%) → 3S↓ + 2NO↑ + 4H2O
- PbS + 8HNO3 (đặc) → PbSO4↓ + 8NO2↑ + 4H2O
HNO3 được sản xuất bằng cách nào?
HNO3 tồn tại trong tự nhiên
Axit nitric không bền về bản chất và không thể tồn tại lâu dài trong tự nhiên, nhưng sự hình thành axit nitric là một phần của chu trình nitơ, sự hình thành HNO3 trong tự nhiên gồm 3 quá trình sau dây
- N2 + O2 → NO
– Quá trình tạo thành khí nitơ đioxit
- 2NO + O 2 → 2NO2
- 3NO2 + H2O → 2HNO 3 + NO

(HNO3 68% Hàn Quốc quy cách 280kg/phuy)
Trong phòng thí nghiệm HNO3 được điều chế như thế nào?
– Cho KNO3 phản ứng với acid sunfuric (H2SO4) 96%, và chưng cất hỗn hợp này tại nhiệt độ sôi của acid nitric là 83 ℃ cho đến khi còn lại chất kết tinh màu trắng của kali bisunfat (KHSO4) còn lại trong bình.
- H2SO4 + KNO3 → KHSO4 + HNO3
Sản xuất HNO3 trong công nghiệp
– Việc sản xuất acid nitric được thực hiện bằng công nghệ Ostawald do Wilhelm Ostwald phát minh, pha trộn nitơ dioxide (NO2) và nước với sự có mặt của oxy hoặc sử dụng không khí để oxy hóa HNO2 cũng tạo ra acid nitric
- 4NO2 + O2 + 2H2O → 4HNO3
Ứng dụng của Axit nitric HNO3
– Khoảng 75 đến 80% lượng HNO3 trên thế giới sản xuất ra được sử dụng để sản xuất phân bón như: phân đạm một lá nitrat amoni.
– HNO3 được dùng làm thuốc thử trong phòng thí nghiệm và trường học.

(HNO3 được sử dụng trong ngành CN luyện kim)
– HNO3 68% được sử dụng để sản xuất thuốc nổ bao gồm nitroglycerin, trinitrotoluen (TNT) và cyclotrimethylenetrinitramin (RDX)
– Axit nitric còn được dùng trong ngành luyện kim: trước hết oxi hóa kim loại không tinh khiết thành nitrat, loại bỏ tạp chất rồi khử, HNO3 có thể oxy hóa sắt mà không bị ăn mòn thêm.
– Axit nitric 68% là chất trung gian để sản xuất các chất hữu cơ, bột màu, sơn, thuốc nhuộm vải và thuốc tẩy màu. Và là thành phần quan trọng của thuốc trừ sâu.
Những lưu ý khi sử dụng Axit Nitric HNO3
– Axit nitric có tính oxy hóa và ăn mòn ở cả dung dịch đậm đặc và loãng nên rất nguy hiểm cho con người, bắn vào da, mắt có thể gây bỏng nặng. Sau khi da tiếp xúc với axit nitric sẽ từ từ chuyển sang màu vàng, cuối cùng lớp biểu bì bị ố vàng sẽ bong ra (do axit nitric và protein tiếp xúc sẽ gây ra phản ứng xanthin và biến tính).
(Ảnh axit nitric được lữu giữ tại kho)
– Hít phải khí của axit nitric lỏng có thể gây kích ứng đường hô hấp và có thể gây phù phổi cấp tính. Nếu uống nhầm hóa chất này gây đau bụng dữ dội. Trong trường hợp nghiêm trọng, có thể gây thủng dạ dày, co thắt thanh quản, tổn thương thận, sốc và ngạt thở.
– Bảo quản HNO3 trong kho mát, thông gió. Tránh xa lửa và nguồn nhiệt. Nhiệt độ bảo quản không vượt quá 30 ℃ và độ ẩm tương đối không vượt quá 80%, bình chứa phải đạy nắp kín. Nó nên được bảo quản riêng biệt với các chất khử, kiềm, và kim loại kiềm.